EU
Lýðheilsa: Sterkari reglur um lækningatæki
Útgefið
3 árumon

Nýjar reglur ESB um lækningatæki (MDR) taka gildi og koma á nútímalegri og öflugri regluverki til að vernda lýðheilsu og öryggi sjúklinga. Nýju reglurnar byrja að gilda eftir eins árs frestun vegna fordæmalausra áskorana um faraldursveirufaraldur og taka á þörfinni fyrir aukið framboð af mjög mikilvægum lækningatækjum víða um ESB.
Reglugerðin nær til lækningatækja, allt frá mjöðmskiptum til límandi plástra. Það eykur gegnsæi og færir löggjöf ESB í takt við tækniframfarir og framfarir í læknavísindum. Það bætir klínískt öryggi og skapar sanngjarnan markaðsaðgang fyrir framleiðendur.
Stella Kyriakides, Framkvæmdastjóri heilbrigðis- og matvælaöryggis, sagði: „Þetta er mikilvægt framfaraskref til verndar sjúklingum um alla Evrópu. Nýju reglurnar bæta öryggi og gæði lækningatækja um leið og þeir veita meira gegnsæi fyrir sjúklinga og minni stjórnsýslubyrði fyrir fyrirtæki. Löggjöfin mun styrkja nýsköpun og alþjóðlega samkeppnishæfni okkar og tryggja að við séum tilbúin fyrir allar nýjar og nýjar áskoranir. “
Í stuttu máli, Reglugerð um lækningatæki:
- Bætir gæði, öryggi og áreiðanleika lækningatækja: það setur hert eftirlit með áhættutækjum eins og ígræðslum og krefst samráðs við sundlaug sérfræðinga á vettvangi ESB áður en lækningatæki eru sett á markað. Klínískt mat, rannsóknir og tilkynntir aðilar sem samþykkja vottun lækningatækja verða undir hertu eftirliti.
- Styrkir gegnsæi og upplýsingar fyrir sjúklinga, svo auðvelt sé að finna mikilvægar upplýsingar. Evrópski gagnagrunnurinn yfir lækningatæki (EUDAMED) mun innihalda upplýsingar um hvert lækningatæki á markaðnum, þar á meðal rekstraraðila og vottorð útgefin af tilkynntum aðilum. Hvert tæki mun hafa einstakt auðkenni tækis svo að það sé að finna í EUDAMED. Ítarlegri merkingar og rafrænar handbækur munu auka notendavæni. Ígræðslusjúklingar fá ígræðslukort með öllum nauðsynlegum upplýsingum.
- Bætir árvekni og markaðseftirlit:Þegar tæki eru fáanleg á markaðnum verða framleiðendur að safna gögnum um afköst tækjanna. ESB-lönd munu samræma náið árvekni þeirra og markaðseftirlit.
Bakgrunnur
Það eru yfir 500,000 tegundir lækningatækja á markaði ESB. Dæmi um lækningatæki eru snertilinsur, röntgenvélar, öndunarvélar, gangráðir, hugbúnaður, brjóstígræðsla, mjaðmaskipti og límandi plástur.
FáðuLækningatæki hafa grundvallar hlutverk í björgun mannslífa með því að veita nýstárlegar heilsugæslulausnir til að greina, koma í veg fyrir, fylgjast með, spá, spá, meðhöndla eða létta sjúkdóma.
Reglugerðin um lækningatæki er bætt við reglugerðina um sjúkdómsgreiningar á sjúkdómsgreiningu (2017/746 / ESB) með gildistökudegi 26. maí 2022. In vitro sjúkdómsgreiningartæki eru notuð til að framkvæma próf á sýnum, þar á meðal eru HIV blóðrannsóknir, meðgöngupróf, COVID-19 próf og blóðsykurskerfi fyrir sykursjúka.
Fyrir meiri upplýsingar
Deildu þessari grein:
EU Reporter birtir greinar frá ýmsum utanaðkomandi aðilum sem lýsa margvíslegum sjónarmiðum. Afstaðan sem tekin er í þessum greinum er ekki endilega afstaða EU Reporter.

Þú gætir eins og

Utanríkismálastjóri ESB gerir sameiginlegan málstað með Bretlandi í alþjóðlegum átökum

Hvers vegna er enn ekki brugðist við ákalli ESB-þingsins um að skrá IRGC sem hryðjuverkasamtök?

Ný brú fyrir unga Evrópubúa beggja vegna Ermarsunds

Áhrif fjöldaflutninga Rússa á þjóðernisspennu í Kirgisistan

Hver er kostnaðurinn við að halda aðildarríkjum frá landamæralausu svæði ESB

Indland vs Kína: hver fær peningana?

Fyrirtæki halda áfram að njóta 5G fríðinda þar sem Wipro og Nokia vinna saman

Kasakstan setur lög sem gera heimilisofbeldi refsivert, sigur fyrir mannlega reisn

Yfirlýsingin „Til varnar lýðræðis“ sameinar miklar reglur og kosningapólitík
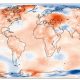
Kópernikus: Hitamet á heimsvísu heldur áfram – apríl 2024 heitasti í sögunni

Meintur Azima tölvuþrjótur handtekinn í London

Bandalag fyrir milljarð: Ihor Kolomoisky, Bank Alliance & United Energy

14 milljarða evra af óreglulegum útgjöldum ESB frá 2014 til 2022

Kasakstan sameinist um að takast á við flóðakreppuna

Fjöldi kaupenda yfir landamæri í Vestur-Evrópu mun slá met árið 2025

Sjálfbærar umbúðir gætu tafið áhrif sorpsmyndunar í Evrópu

Tvær lotur 2024 hefjast: Hér er hvers vegna það skiptir máli

Nýársskilaboð Xi Jinping forseta 2024

Hugvekjandi ferð um Kína

Áratugur BRI: Frá framtíðarsýn til veruleika

"Sneaking Cults" - Verðlaunuð heimildarmynd sem tókst vel í Brussel

Trúarbrögð og réttindi barna - Álit frá Brussel

Yfir 100 kirkjumeðlimir barðir og handteknir við tyrknesku landamærin

Dýpka orkusamstarfið við Aserbaídsjan - áreiðanlegan samstarfsaðila Evrópu fyrir orkuöryggi.
Stefna
-

 Common Foreign og öryggismál4 dögum
Common Foreign og öryggismál4 dögumUtanríkismálastjóri ESB gerir sameiginlegan málstað með Bretlandi í alþjóðlegum átökum
-

 Íran3 dögum
Íran3 dögumHvers vegna er enn ekki brugðist við ákalli ESB-þingsins um að skrá IRGC sem hryðjuverkasamtök?
-

 Brexit2 dögum
Brexit2 dögumNý brú fyrir unga Evrópubúa beggja vegna Ermarsunds
-

 Kirgisistan3 dögum
Kirgisistan3 dögumÁhrif fjöldaflutninga Rússa á þjóðernisspennu í Kirgisistan
